Accueil > Les critères pour défibrillateurs automatisés externes
Matecir Defibril distribue 5 modèles de DAE / Défibrillateur Automatisé Externe (externe : opposition à l’implantable) et en maintient 34. Avec au 01/01/2024, plus de 18 000 clients, 16 000 DAE (Défibrillateur Automatisé Externe) vendus et 23 500 contrats de maintenances, la société est leader des distributeurs indépendants multi marques.
Dans le cadre de nos certifications
nous avons réalisé une étude approfondie sur les critères essentiels de choix pour équiper une entreprise « Grand Public », soit non professionnelle du secourisme ou de « l’urgentisme ».
Cette étude se veut factuelle, basée sur des constats, des normes, des règles.
Elle permet au décideur de disposer des données essentielles, réglementaires, techniques et financières, préalables à son choix.
Vous trouverez ci-dessous une synthèse imprimable ainsi que la présentation de notre offre de maintenance.
Impression pdf :




Lorsqu’il s’agit de choisir un défibrillateur (défibrillateurs entièrement automatique ou semi-automatique), plusieurs critères doivent être pris en compte pour garantir son efficacité. Il est essentiel de sélectionner un modèle adapté à l’environnement et à l’utilisateur. Les défibrillateurs modernes délivrent des chocs sur le cœur de manière automatique, ce qui permet de prendre les bonnes décisions rapidement. En cas d’arrêt cardiaque, il est crucial d’agir vite (donner l’alerte et effectuer un massage cardiaque) pour maximiser les chances de survie. Un défibrillateur, dispositif de premiers secours, permet de guider l’utilisateur grâce à des instructions vocales et visuelles pour effectuer correctement les manœuvres nécessaires. Il analyse le rythme cardiaque et décide si un choc est nécessaire, offrant ainsi un soutien vital jusqu’à l’arrivée des secours. Choisir un défibrillateur fiable et facile à utiliser peut faire la différence entre la vie et la mort.
DAE : Défibrillateur Automatisé Externe. Terme générique. Externe est utilisé en opposition au défibrillateur implantable.
DSA : Le DAE est en mode Semi-Automatique. Il demandera au témoin sauveteur d’appuyer sur le bouton « choc »
DEA : Le DAE est en mode Entièrement Automatique. Il enverra le choc, si nécessaire, sans intervention humaine, après avoir prévenu de ne plus toucher la victime.
Un DAE dispose de sa propre source d’énergie. Il est donc mobile dans tous les cas.
Un DAE ne « s’installe » pas. Du fait de sa mobilité, vous pouvez le placer où bon vous souhaite. Pour preuve, de nombreuses collectivités ont déjà fait le choix d’équiper les voitures de police municipale. Seul, le boitier demandera une installation.
Pour un boitier intérieur, il s’agit alors d’une prestation de « bricolage », avec 3 trous à percer, 3 chevilles et 3 vis.
Pour une installation du défibrillateur dans un boitier extérieur, donc avec un boitier chauffant, il y aura alors un « pré requis » obligatoire avec l’apport d’une ligne électrique. Vous aurez alors tout intérêt à attendre la livraison du boitier, et faire réaliser l’apport de la ligne, le branchement et la fixation du boitier par le même professionnel, ce qui vous coutera au final nettement moins cher que deux prestations séparées.
Dans les deux cas, l’exploitant doit tenir compte de l’obligation de signalisation (kit signalétique et géolocalisation) du défibrillateur. sera dans l’obligation de signaler la présence du défibrillateur.
Quasiment tous les DAE présents sur le marché supportent une température de stockage comprise entre -30°C et + 50°C. MAIS ce n’est pas le cas des électrodes, enduites d’un gel adhérent à la peau et composé à plus de 90% d’eau.
Ce gel durcira en cas de température négative, ou se liquéfiera en cas de température trop élevée (>40°C). Dans les 2 cas, les électrodes ne seront pas opérationnelles, et de fait, le DAE sera inutile. Si le risque existe, il est donc impératif que le DAE soit placé dans un boitier chauffant et ventilant, sans exposition trop prolongée au soleil afin d’éviter « l’effet de serre ».
Un projet de loi est à l’étude afin de renforces les modalités concrètes des obligations de maintenance des défibrillateurs automatisés externes. Ce projet de loi précise deux notions importantes:
« Tout instrument, appareil, équipement, matière ou autre article, utilisé seul ou en association, y compris le logiciel nécessaire pour le bon fonctionnement de celui-ci, destiné par le fabricant à être utilisé chez l’homme à des fins :
et dont l’action voulue dans ou sur le corps humain n’est pas obtenue par des moyens pharmacologiques ou immunologiques ni par métabolisme, mais dont la fonction peut être assistée par de tels moyens ».
Elles sont fondées sur la vulnérabilité du corps humain en tenant compte des risques potentiels liés à la conception technologique et à la fabrication des dispositifs.
La réglementation actuelle de l’Union Européenne en matière de dispositifs médicaux se compose de la directive 90/385/CEE du Conseil relative aux dispositifs médicaux implantables actifs (DDMIA) et de la directive 93/42/CEE du Conseil sur les dispositifs médicaux (DDM).
La DDM répartit les produits dans quatre classes de risque :
Les dispositifs médicaux implantables actifs (tels que les stimulateurs cardiaques et les défibrillateurs implantables) qui relèvent de la DDMIA appartiennent de facto à la classe III.
Cette réglementation était en cours de révision depuis 2012, le Parlement européen ayant demandé à la Commission européenne de renforcer la réglementation afin de garantir au mieux la sûreté des technologies médicales, suite notamment au scandale des implants mammaires PIP.
En 2012, la Commission a donc présenté une proposition législative comprenant un vaste ensemble de mesures visant à moderniser la réglementation actuelle.
La nouvelle réglementation a été publiée au JOUE Journal Officiel de l’Union Européenne le 5 mai 2017.
Elle est applicable depuis le 5 mai 2021 (initialement 05/05/2020, report suite à la crise sanitaire).
Les DAE jusqu’alors en classe IIb font l’objet d’une reclassification dans la catégorie de risque la plus élevée (Classe III).
https://eur-lex.europa.eu/legal-content/FR/TXT/PDF/?uri=CELEX:32017R0745&from=FR
Page 145, paragraphe 7.9, règle 22

À compter de mai 2021, tous les nouveaux marquages C.E ou le renouvellement des marquages C.E existants se feront à partir des conditions techniques de la classe III.
Tous les DAE existants devront renouveler leur marquage C.E avant mai 2024.
Tous les fabricants peuvent affirmer que leur DAE est en classe III, et ce même si le marquage CE obtenu l’a été sur les considérations techniques de la classe IIb. Le renouvellement du marquage C.E de leur DAE se fera, ou non, sur les bases de la classe III, à la fin de leur marquage CE, au plus tard en mai 2024.
La législation proposée permettra de renforcer le contrôle des produits avant leur mise sur le marché et d’intensifier leur surveillance après leur commercialisation. Elle vise également à renforcer l’évaluation clinique des produits à risque plus élevé et à créer un système d’identification unique des dispositifs médicaux, grâce auquel il serait possible de rappeler plus facilement les produits défectueux.
Pour renforcer la sécurité d’utilisation des dispositifs médicaux, le nouveau règlement soumet désormais les fabricants à l’obligation de disposer d’un système de gestion de la qualité qui garantit la traçabilité du dispositif médical tout au long de la chaîne de distribution, jusqu’à l’utilisateur final.
Le nouveau règlement incite ainsi le fabricant à une vigilance particulière en termes de sélection de ses distributeurs. En effet, si les informations et documents que le fabricant communique aux Autorités de santé sont incomplets ou incorrects (rapport annuel notamment) et/ou si les actions correctives sont jugées insuffisantes, les autorités peuvent interdire ou limiter la commercialisation du dispositif ainsi que rappeler ou retirer le dispositif dudit marché, afin de garantir la protection de la santé publique et la sécurité du patient.
Ces nouvelles contraintes vont avoir 3 impacts quasi immédiats :
-1 Il est probable que la majorité des fabricants sans réelle représentation française, ou au minimum européenne, ne soient plus sur le marché d’ici 4 ou 5 ans,
-2 Les fabricants sérieux vont exiger d’importantes garanties qualitatives de la part de leurs distributeurs Certains fabricants ont déjà annoncé leur intention de ne collaborer qu’avec des distributeurs certifiés ISO à partir de 2022,
-3 Ce nouveau règlement va ainsi condamner les sous-traitances de maintenance allouées par des distributeurs sans effectif à des structures de formation, qui, outre le fait que les intervenants sont anonymes et rarement salariés, ne sont quasiment jamais assurées pour ce type d’activité.
Matecir Defibril a fait le choix de ne distribuer que des DAE produits par des fabricants faisant la démonstration d’une présence soutenue sur le marché hospitalier européen à travers une gamme étendue de produits.
Un fabricant dont la gamme de produits comprend des moniteurs, des défibrillateurs professionnels (débrayables) et « grand public (automatisé externe), et des électrocardiographes (ECG) aura une démarche générale pour l’ensemble des produits, gage de garantie. Le coût des études et des processus spécifiques de production, d’assurance qualité et de rappel sera global, pour un marché de plusieurs centaines de millions d’euros.
A contrario, un fabricant dédié au seul DAE « grand public » sera confronté à un coût d’étude très important pour un seul type de produit.
Soyez vigilant : Un fabricant qui n’obtiendra pas son marquage CE sur les bases de la classe III stoppera très probablement la production de son appareil. Il vous sera alors très difficile, voire impossible, de trouver des consommables et vous n’aurez alors pas d’autre solution que de changer le DAE
Les marques avec lesquelles nous travaillons sont spécialisées dans la cardiologie, et non dans l’électronique. Il est aisé de comparer les « gammes produits » des fabricants en analysant leur capacité à fournir d’autres produits destinés à la cardiologie professionnelle, du Samu aux hôpitaux en passant par les SDIS (Sapeurs-pompiers). Nous ne travaillons pas avec les marques « mono produit » visant seulement un marché de niche.
Qu’il s’agisse d’une voiture, d’une photocopieuse ou de n’importe quel objet domestique, chaque produit présente des arguments positifs et d’autres qui le sont moins.
Il y a néanmoins des pièges flagrants à éviter.
Plusieurs DAE sont munis d’une pile interne communément appelée « pile de sauvegarde » ou « pile mémoire ». Si c’est le cas, il y aura obligatoirement une intervention technique avec ouverture de la structure du DAE pour remplacer cette pile « interne ». Dans le cas contraire cela peut nuire à la performance du défibrillateur.
La fréquence de ce remplacement est fonction du fabricant, mais est généralement, et logiquement pour une pile de 9V, de l’ordre de 6 ans. Cette opération obligatoire, généralement facturée entre 200 et 350€ H.T. alourdira le budget de fonctionnement. N’hésitez pas à poser la question.
Il est absolument impératif que le DAE détecte si les électrodes sont correctement connectées et informe dans le cas contraire. En toute logique, un DAE ne devrait pas être en mesure de poursuivre l’analyse et/ou le massage cardiaque si les électrodes ne sont pas connectées. N’hésitez pas à poser la question.
Nous refusons de commercialiser de tels produits.
Si l’ouverture du capot déclenche le fonctionnement du DAE, sa fermeture accidentelle ne doit en aucun cas provoquer l’arrêt du DAE.
N’hésitez pas à poser la question. Nous refusons de commercialiser de tels produits.
Pour nous contacter ou à demander un devis.
De nombreuses marques proposent des DAE « nus », avec batterie (ou piles) et électrodes adulte, mais sans les accessoires du défibrillateur pourtant indispensables, qui viendront donc s’ajouter au prix de l’appareil.
– La sacoche de transport
La victime ne choisira pas l’endroit où elle fera son malaise cardiaque. Dans 99% des cas, il sera nécessaire de transporter en urgence le défibrillateur sur le lieu où se trouve la victime.
Il est donc impératif que le défibrillateur soit dans une sacoche. Le prix de cette sacoche doit être intégré dans le pack.
– Le kit de 1ers secours
La présence d’un kit de 1ers secours contenant : un rasoir (pilosité pour pose des électrodes), des ciseaux (découpe des vêtements), une paire de gants (si saignement), une serviette sèche (si humidité ou transpiration), un masque d’insufflation, une compresse alcoolisée, est impérative. Le prix de ce kit doit être intégré dans le pack.
Il est démontré que les DAE de qualité correctement maintenus ont une durée de vie de 12 ans et plus. Pour acheter aux meilleures conditions, vous devez valider deux budgets : l’achat et le fonctionnement, en intégrant les coûts des consommables et des accessoires. En validant ces coûts, vous éviterez le piège dit « de l’imprimante », avec un DAE moins cher puis des consommables hors de prix.
Tous les fabricants ne présentant pas des consommables ayant la même durée de vie.
Vous devez tenir compte du ratio prix/durée de vie et établir un budget sur des périodes de 10 ou 15 ans.
Nous vous conseillons de renseigner le tableau suivant :
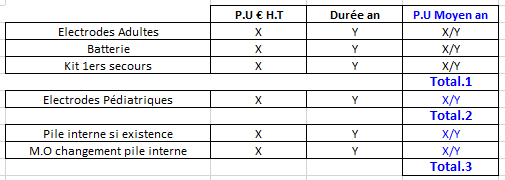
Le défibrillateur automatisé externe est présenté en 2 modes :
– Entièrement automatique (DEA), le défibrillateur enverra le choc sans aucune intervention humaine en cas de nécessité, après avoir prévenu les « témoins sauveteurs » par un message vocal : « choc conseillé dans 3, 2, 1 ».
– Semi automatique (DSA), le témoin sauveteur devra appuyer sur le bouton choc quand l’appareil lui en donnera l’ordre.
L’unique intérêt de ce mode est de vérifier que personne ne touche la victime. Dans ce cas, le choc serait réparti sur 2 personnes et perdrait une grande partie de son efficacité.
Notre conseil
Notre approche est très simple : Si le taux de formation à l’utilisation du défibrillateur de la population susceptible d’intervenir est inférieur à 40%, nous préconisons le mode entièrement automatique. Nous avons pu vérifier lors de simples démonstrations que les personnes non formées hésitaient avant d’appuyer sur le bouton « choc », perdant ainsi un temps précieux.